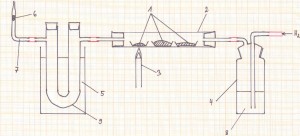
Schülerversuch: Reaktion von Kupfer und Schwefel quantitativ
Dies ist ein sehr bekannter Versuch zum Nachweis vom Gesetz der konstanten Proportionen. Dazu lässt man ein Kupferblech mit bekannter Masse mit Schwefel reagieren und wiegt das Produkt erneut. Dabei ist das Massenverhältnis von Kupfer und Schwefel im Idealfall konstant, da folgende Reaktion abläuft:
2Cu + S → Cu2S
Es reagieren also 32u Schwefel mit ca. 2x63,5u Kupfer (127u) (alle Werte gerundet), sodass man auf ein Massenverhältnis von ziemlich genau 4:1 ( m(Cu):m(S) ) kommt.
Dazu spannt man ein Reagenzglas mit wenig Schwefelpulver leicht schräg in ein Stativ ein. Jede Versuchsgruppe (je mehr Gruppen, desto besser), erhölt ein unterschiedlich großes Kupferblech. Dieses wird gewogen und so in das Reagenzglas eingeführt, dass es etwa 4–5cm über dem Schwefel zu liegen kommt. Dann werden sowohl der Schwefel als auch das Reagenzglas erhitzt. Man sollte den Ablauf dieses Experimentierteils einmal vorher mit den SuS üben (Vorstunde).
Durch eine vorbereitete Schülerhand kann der spannende Teil des Versuches so ablaufen: