Zersetzungsspannung
Alle Elemente streben den energieärmsten Zustand, d.h. eine möglichst stabile Elektronenkonfiguration an. In der Regel ist dieser erreicht, wenn in der äußersten Kugelschale acht Elektronen vorhanden sind. Für die Reaktionen von Zink und Brom ergibt sich folgende Reaktionsgleichung:
Zn + Br2 → ZnBr2
Aufgeschlüsselt nach Teilgleichungen für die Oxidation und Reduktion sieht man, dass dabei Elektronen vom Zink zum Brom fließen:
(1) Zn → Zn2+ + 2e- (Oxidation)
(2) Br2 + 2e- → 2Br- (Reduktion)
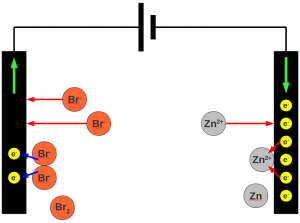
Diese Richtung des Elektronenflusses ist quasi die natürliche: Auf diese Weise erreichen beide Elemente unter Energieabgabe den energieärmsten Zustand. Wenn die Elektronen in die andere Richtung fließen sollen, bedarf es der Zufuhr von Energie, z.B. von elektrischem Strom, den eine „Elektronenpumpe“ wie z.B. eine Batterie liefern kann. Der Prozess lässt sich etwa in einer Elektrolysezelle umkehren, die eine wässrige Lösung von Zinkbromid enthält. Als Elektrodenmaterial dient Graphit – die Wahl dieses Materials ist nicht beliebig. Eine solche Zelle könnte folgendermaßen aufgebaut sein:
Die negativ geladenen Bromidionen werden vom Pluspol (Anode) der Elektrolysezelle angezogen und dort unter Abgabe eines Elektrons entladen. Der Prozess (2) läuft „rückwärts“. Analog werden die Zinkionen von dem Minuspol (Kathode) angezogen und dort unter Aufnahme von Elektronen entladen. Der Prozess (1) läuft „rückwärts“. Beide Prozesse müssen durch eine externe Spannungsquelle erzwungen werden, sodass Elektronen an der Kathode eintreten und an der Anode austreten können (grüne Pfeile).